Fermentai
apibrėžimas
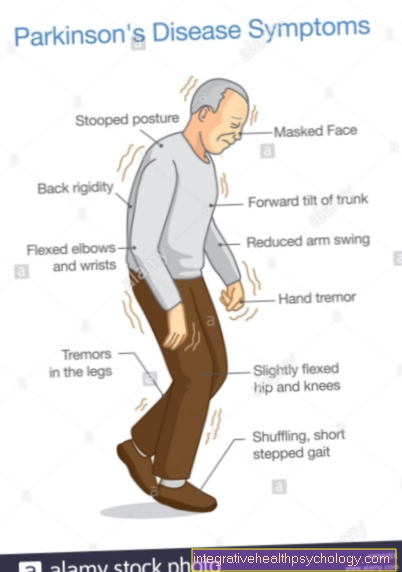
Fermentai yra cheminės medžiagos, kurias galima rasti visame kūne. Jie nustato organizme vykstančias chemines reakcijas.
istorija
Žodis fermentas buvo iš Vilhelmas Friedrichas Kühne'as 1878 m ir yra kilęs iš graikų kalbos žodžio enzmon, reiškiančio mieles ar rūgštynes. Tada tai rado kelią į tarptautinį mokslą. tarptautinė grynosios chemijos sąjunga (IUPAC) ir tarptautinė biochemijos sąjunga (IUBMB) parengė fermentų nomenklatūrą, apibrėžiančią šios didelės grupės medžiagų atstovus kaip bendrą grupę. Pavadinimas, pagal kurį fermentai klasifikuojami pagal jų užduotis, yra svarbus nustatant atskirų fermentų užduotis.
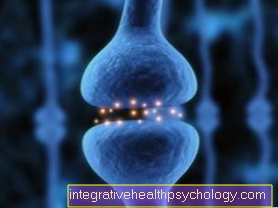
Fermentų iliustracija
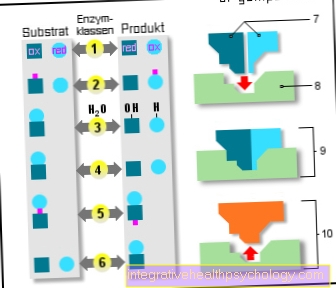
Fermentai
6 fermentų klasės:
- Oksidoreduktazės
(Oksidacija / redukcija) - Transferazės
(Užkrato pernešimas) - Hidrolazės
(Vandens naudojimas) - Lizazės
(Išpjaustymas) - Izomerazės
(ta pati molekulinė formulė) - Ligazės
(Papildomos reakcijos) - Substratai
- Aktyvus centras
- Fermentas / substratas
sudėtingas - Fermentas / produktas
sudėtingas
Visų apžvalgaDr-Gumpert atvaizdus galite rasti: medicininės iliustracijos
Pavadinimas
Pavadinimas fermentas įjungtas trys pagrindiniai principai pagrįstas.Fermentų pavadinimai, kurie baigiasi inaze, apibūdina kelis fermentus sistemoje. Pats fermento pavadinimas apibūdina reakciją, kurią fermentas pradeda judėti (katalizuojamas). Fermento pavadinimas taip pat yra fermento klasifikacija. Be to, kodų sistema, kuri EB numerio sistema, kuriame fermentai gaminami skaitmeniniu kodu keturi skaičiai galima rasti. Pirmasis skaičius nurodo fermento klasę. Visų aptiktų fermentų sąrašai užtikrina, kad nurodytą fermento kodą galima rasti greičiau. Nors kodai yra pagrįsti reakcijos, kurią fermentas katalizuoja, savybėmis, iš tikrųjų skaitmeniniai kodai yra sunkūs. Dažniau naudojami sisteminiai pavadinimai, pagrįsti aukščiau pateiktomis taisyklėmis. Problemos dėl nomenklatūros kyla, pavyzdžiui, su fermentais, kurie katalizuoja kelias reakcijas. Todėl kartais jiems yra keli vardai. Kai kurie fermentai turi trivialius pavadinimus, kurie nenurodo, kad minima medžiaga yra fermentas. Kadangi vardai buvo tradiciškai plačiai naudojami, kai kurie iš jų buvo išsaugoti.
Klasifikacija pagal fermento funkciją
Pagal IUPAC ir IUBMB, fermentai yra suskirstyti į šešias fermentų klases pagal jų inicijuotą reakciją:
- Oksidoreduktazės
Oksidoreduktazės sukėlė redokso reakcijas. Šioje cheminėje reakcijoje elektronai pereina iš vieno reakcijos partnerio į kitą. Yra vienos medžiagos elektronų išsiskyrimas (oksidacija) ir kitos medžiagos elektronų įsisavinimas (redukcija).
Katalizuojamos reakcijos formulė yra A? + B? A? + B ?.
Medžiaga A išskiria elektroną (?) Ir yra oksiduota, o medžiaga B absorbuoja šį elektroną ir yra redukuojama. Štai kodėl redokso reakcijos taip pat vadinamos redukcijos-oksidacijos reakcijomis.
Daugelis metabolinių reakcijų yra redoksinės reakcijos. Deguigenazės perduoda savo substratui vieną ar daugiau deguonies atomų. - Transferazės
Transferazės perduoda funkcinę grupę iš vieno substrato į kitą. Funkcinės grupės yra organinių junginių atomų grupės, kurios didžiąja dalimi nulemia medžiagos savybes ir reakciją. Cheminiai junginiai, turintys tas pačias funkcines grupes, dėl panašių savybių yra suskirstyti į medžiagų klases. Funkcinės grupės bus suskirstytos pagal tai, ar jie yra heteroatomai, ar ne. Visi heteroatomai yra organinių junginių atomai, kurie nėra nei anglis, nei vandenilis.
Pvz .: -OH -> hidroksilo grupė (alkoholiai) - Hidrolazės
Hidrolazės skaido ryšius į grįžtamas reakcijas, naudodamos vandenį. Esteriai, esteriai, peptidai, glikozidai, rūgšties anhidridai arba C-C jungtys. Pusiausvyros reakcija yra tokia: A-B + H2O? A-H + B-OH.
Fermentas, priklausantis hidrolazių grupei, yra pvz. Alfa galaktozidazė. - Lizazės
Lizazės, dar vadinamos sintazėmis, katalizuoja sudėtingų produktų skaidymąsi iš paprastų substratų, neskaidydamos ATP. Reakcijos schema yra A-B → A + B.
ATP yra adenozino trifosfatas ir nukleotidas, susidedantis iš nukleozido adenozino trifosfato (ir tokiu būdu daug energijos turinčios nukleorūgšties RNR). Tačiau ATP daugiausia yra universali betarpiškai prieinamos energijos forma kiekvienoje ląstelėje ir tuo pat metu svarbus energijos tiekimo procesų reguliatorius. Jei reikia, ATP sintetinamas iš kitų energijos atsargų (kreatino fosfato, glikogeno, riebalų rūgščių). ATP molekulę sudaro adenino liekana, cukraus ribozė ir trys fosfatai (nuo β iki) esteryje (α) arba anhidridiniai ryšiai (β ir α). - Izomerazės
Izomerazės pagreitina izomerų cheminį virsmą. Izomerizmas yra dviejų ar daugiau cheminių junginių, turinčių lygiai tuos pačius atomus (ta pati empirinė formulė) ir molekulinis svoris, atsiradimas, kurie vis dėlto skiriasi atomų ryšiu ar erdviniu išdėstymu. Atitinkami junginiai vadinami izomerais.
Šie izomerai skiriasi savo cheminėmis ar (ir) fizikinėmis, o dažnai ir biocheminėmis savybėmis. Izomerija pirmiausia pasireiškia organiniais junginiais, bet taip pat ir (neorganiniais) koordinavimo junginiais. Izomerija yra padalinta į skirtingas sritis. - Ligazės
Ligazės katalizuoja medžiagų, kurios yra chemiškai sudėtingesnės nei naudojamos substratai, susidarymą, tačiau, priešingai nei lizės, fermentiniu būdu yra veiksmingos tik skaidydamos ATP. Taigi šioms medžiagoms formuotis reikalinga energija, kuri gaunama padalijus ATP.
Kai kurie fermentai sugeba katalizuoti keletą, kartais labai skirtingų, reakcijų. Jei taip yra, jie priskiriami kelioms fermentų klasėms.
Galbūt jus taip pat domina šie straipsniai:
- Alfa-gliukozidazė
- Lipazė
- Tripsinas
Klasifikacija pagal fermento struktūrą
Beveik visi fermentai yra baltymai ir gali būti klasifikuojami pagal baltymų grandinės ilgį:
- Monomerai
Fermentai, kuriuos sudaro tik viena baltymų grandinė - Oligomerai
Fermentai, sudaryti iš kelių baltymų grandinių (monomerų) - Kelių fermentų grandinės
Keli agreguoti fermentai, kurie bendradarbiauja ir reguliuoja vienas kitą. Šios fermentų grandinės katalizuoja nuoseklius ląstelės metabolizmo etapus.
Be to, yra atskiros baltymų grandinės, turinčios keletą fermentų aktyvumų, jie vadinami daugiafunkciais fermentais.
Klasifikacija pagal kofaktorius
Kita klasifikacija yra klasifikacija atsižvelgiant į kofaktorius. Kofaktoriai, koenzimai ir kofermentai yra skirtingos klasifikacijos medžiagų, kurios daro įtaką biocheminėms reakcijoms per jų sąveiką su fermentais.
Nagrinėjamos organinės molekulės ir jonai (dažniausiai metalo jonai).
Grynus baltymų fermentus sudaro tik baltymai, o aktyvusis centras yra suformuotas tik iš aminorūgščių liekanų ir peptido stuburo. Amino rūgštys yra organinių junginių, turinčių bent vieną karboksigrupę (-COOH) ir vieną amino grupę (-NH2), klasė.
Holoenzimus sudaro baltymo komponentas, apoenzimas, ir kofaktorius, mažos molekulinės masės molekulė (ne baltymas). Abi kartu yra svarbios fermento funkcijai.
Koenzimai
Organinės molekulės, kaip kofaktoriai, vadinamos kofermentais. Jei jie yra kovalentiškai surišti su apoenzimu, jie vadinami protezavimo grupėmis arba kofermentais. Protezo grupė yra terminas, naudojamas apibūdinti nebaltyminius komponentus, tvirtai (paprastai kovalentiškai) surištus su baltymu, turinčiu katalizinį poveikį.
Kosubstratai yra įvairių klasifikacijų medžiagų, turinčių įtakos biocheminėms reakcijoms dėl jų sąveikos su fermentais, pavadinimai. Kaip biokatalizatoriai, molekulės pagreitina reakcijas organizmuose, fermentai pagreitina biochemines reakcijas. Jie sumažina aktyvacijos energiją, kurią reikia įveikti, kad medžiaga galėtų virsti.